课题4 化学式与化合价
一、什么是化学式?
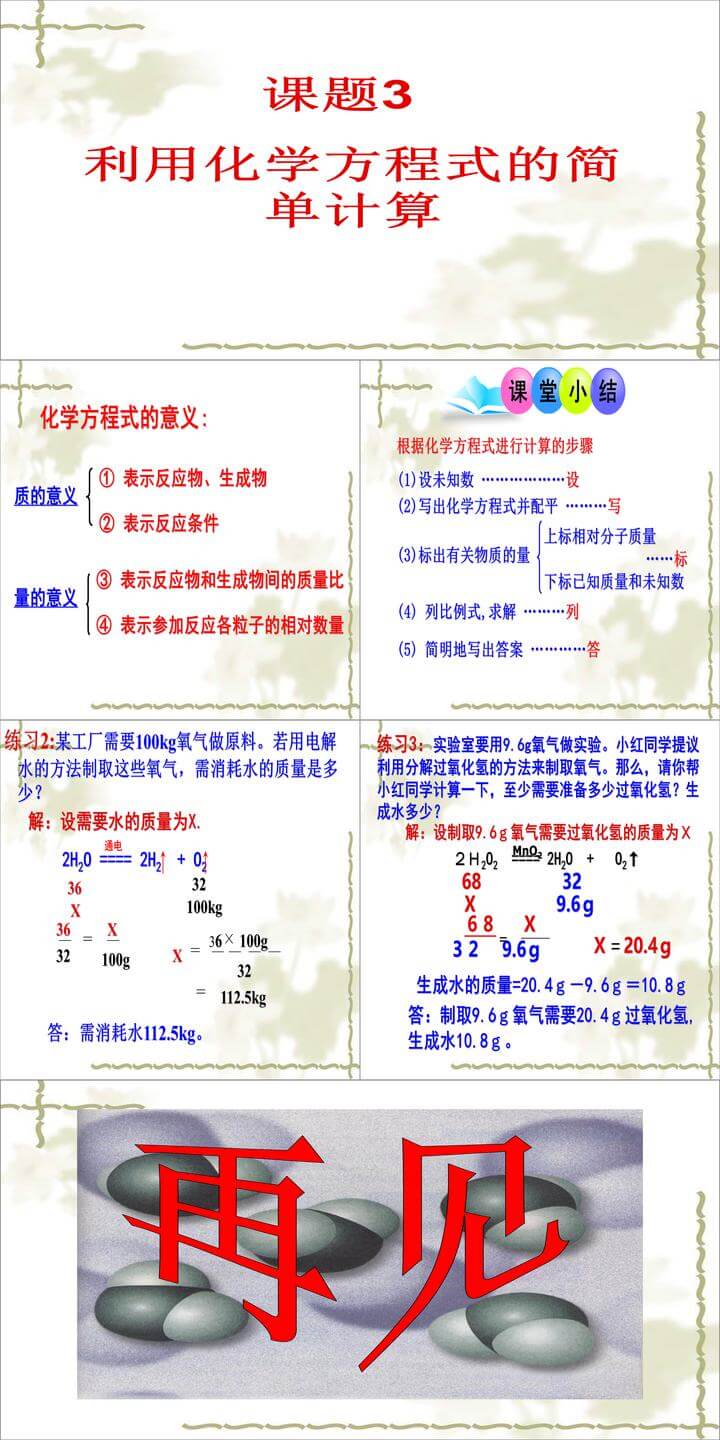
1. 定义:用元素符号和数字的组合表示物质组成的式子。例如,H2O表示水。
2. 化学式的意义:
(1)表示一种物质。
(2)表示物质的组成元素。
(3)对由分子构成的物质来说,表示一个分子。
(4)表示分子的构成。
说出:符号H、2H、H2、2H2各具有什么意义?
H: 表示氢元素;表示1个氢原子。
2H: 表示2个氢原子。
H2: 表示氢气这种物质;表示氢气是由氢元素组成的,表示1个氢分子;表示一个氢分子由2个氢原子构成的。
2H2: 表示2个氢分子。
化学式的书写:
单质的书写:稀有气体、金属和固体非金属、非金属气体。
化合物的书写与读法见P84。
二、化合价
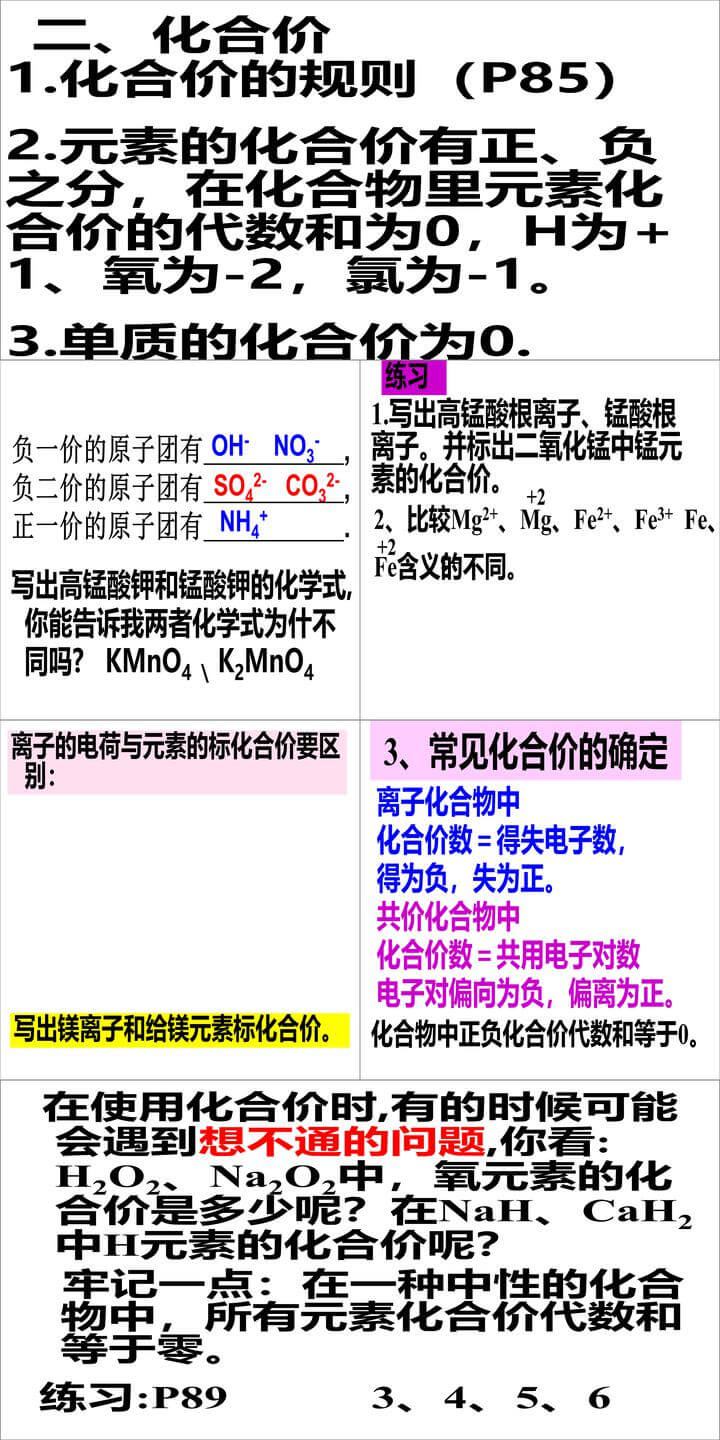
化合价的规则(P85):
元素的化合价有正、负之分,在化合物里元素化合价的代数和为0,例如H为+1、氧为-2,氯为-1。单质的化合价为0。
常见元素化合价的口诀:
一价氢锂钠钾银,
二价氧钙镁钡锌,
三铝四硅五价磷,
二三铁,二四碳,
二四六硫都齐全,
铜汞二价最常见。
记住常见21种元素的化合价和五种原子团的化合价。
负一价的原子团有OH-、NO3-等,负二价的原子团有SO42-、CO32-等,正一价的原子团有NH4+等。
写出高锰酸钾和锰酸钾的化学式,KMnO4 和 K2MnO4,两者化学式不同是因为锰元素的化合价不同。
化合价的应用:
(1)据化合价写化学式,排顺序(正价左,负价右),标价数,价交叉并化简,检查(正负化合价代数和是否为0)。
练习:
1. +5价氮的氧化物的化学式。
2. +6价硫的氧化物的化学式。
3. 练一练见P86(最下方)。
4. 氢氧化钠、氢氧化镁、硫酸锌、硫酸铝、碳酸铵。
写出高锰酸根离子、锰酸根离子,并标出二氧化锰中锰元素的化合价。
比较Mg2+、Mg、Fe2+、Fe3+、Fe的含义的不同。
离子的电荷与元素的标化合价要区别,写出镁离子和给镁元素标化合价。
分别写出2个镁原子、3个镁离子、3个亚铁离子、2个铁离子。
用符号表示下列粒子,并画出相应的结构示意图:
(1)铝离子带三个单位正电荷。
(2)带两个单位正电荷的钙离子。
(3)硫离子带两个单位的负电荷。
(4)氢离子带一个单位正电荷。
常见化合价的确定:
离子化合物中化合价数=得失电子数,得为负,失为正。
共价化合物中化合价数=共用电子对数,电子对偏向为负,偏离为正。
化合物中正负化合价代数和等于0。
练习:
1. 离子化合物硫化钠的化学式为Na2S,在硫化钠中,1个硫原子得2个电子,硫元素为-2价。1个钠原子失1个电子,钠元素为+1价。
2. 共价化合物硫化氢的化学式为H2S,在硫化氢中,1个氢原子与硫原子共用电子对的数目是1,1个硫原子与氢原子共用电子对的数目是2,共用电子对偏离氢、偏向硫,氢元素为+1价,硫元素为-2价。
在使用化合价时,可能会遇到想不通的问题,例如:
H2O2、Na2O2中,氧元素的化合价是多少?
在NaH、CaH2中,H元素的化合价是多少?
练习见P89 3、4、5、6。
牢记一点:在一种中性的化合物中,所有元素化合价代数和等于零。
A、总结化学式的写法:
1. 单质:(1)直接写元素符号;(2)元素符号右下角加2:氟、氯、溴、碘、氮、氢、氧的单质。
2. 化合物:正价左、负价右,读与写的顺序相反。
B、化合价的应用:
根据化学式推求某元素的化合价,例如求KClO3中氯元素的化合价。
练习见书P85 3、4,标出下列物质中各元素的化合价:SiO2、MgO、SO3、CO2、K2O、AgCl、Cu、H2、NaOH、O2。
求次氯酸钾、高锰酸钾、锰酸钾、硫酸、碳酸钠中有变价元素的化合价。
相对分子质量:化学式中各原子的相对原子质量的总和,符号为Mr,又叫化学式的式量。相对分子质量是一个分子的相对质量,也是以一个碳-12原子质量的1/12为标准。
三、有关相对分子质量的计算:
1. 计算相对分子质量即化学式的式量,或若干分子的式量和。例如:Mr(O2) = 16×2 = 32,即氧分子的相对分子质量为32。
2. 计算水H2O的相对分子质量:Mr(H2O) = 1×2 + 16 = 18,H2O的相对分子质量为18。
3. 计算2H2O的相对分子质量的和:2Mr(H2O) = 2×(1×2 + 16) = 18×2 = 36。
练习:
1. 计算高锰酸钾的相对分子质量:Mr(KMnO4) = 39 + 55 + 16×4 = 158,高锰酸钾的相对分子质量为158。
2. 计算下列物质中各元素的质量比:CO2、Fe2O3、CO(NH2)2、NH4NO3、NH4HCO3。
从化学式MnO2中可获得的信息:
(1)组成的元素;
(2)原子间的个数比;
(3)原子的总个数。
二氧化锰中锰元素与氧元素的质量比是多少?
计算下列物质中各元素的质量比:
CO2、Fe2O3、CO(NH2)2、NH4NO3、NH4HCO3。
知道元素间的质量比的表示方法,我们还能知道某元素的质量分数吗?例如二氧化锰中锰元素与氧元素的质量比是55:32,那么二氧化锰中氧元素的质量分数为多少?自学P85例题。
计算物质中某元素的质量分数:
元素的质量分数 = (相对原子质量×原子个数) / 相对分子质量 × 100%。
计算硝酸铵NH4NO3中氮元素的质量分数。
从前面计算知硝酸铵中氮元素的质量分数为35%,那么100克硝酸铵中含氮元素的质量是多少?30克硝酸铵呢?70克硝酸铵呢?据此你能得出什么公式呢?
元素质量与物质质量互算:
元素质量 = 物质质量 × 元素的质量分数。
练习:
1. 150克SO3中含氧元素多少克?
2. 多少克CO(NH2)2中含氮元素70克?
5. 元素含量的相当问题:
(1)1吨NH4NO3与多少吨NH4HCO3的含氮元素质量相等?
(2)120吨CO(NH2)2与多少吨SO3的含氧量相当?
名称:第四单元自然界的水:课题4化学式与化合价精品PPT课件下载
学科:化学
类型:PPT课件
年级:初中三年级
版本:人教版
页数:32张
大小:106.87 KB
格式:pptx
预览图随机显示 6 页,实际是32页PPT。
下载链接中的资源是rar压缩包,解压缩后是ppt文档。
全站资源VIP会员免费下载。
购买之前建议先检测百度网盘链接是否失效。
部分精品课件来自优质公开课PPT,请勿公开传播。