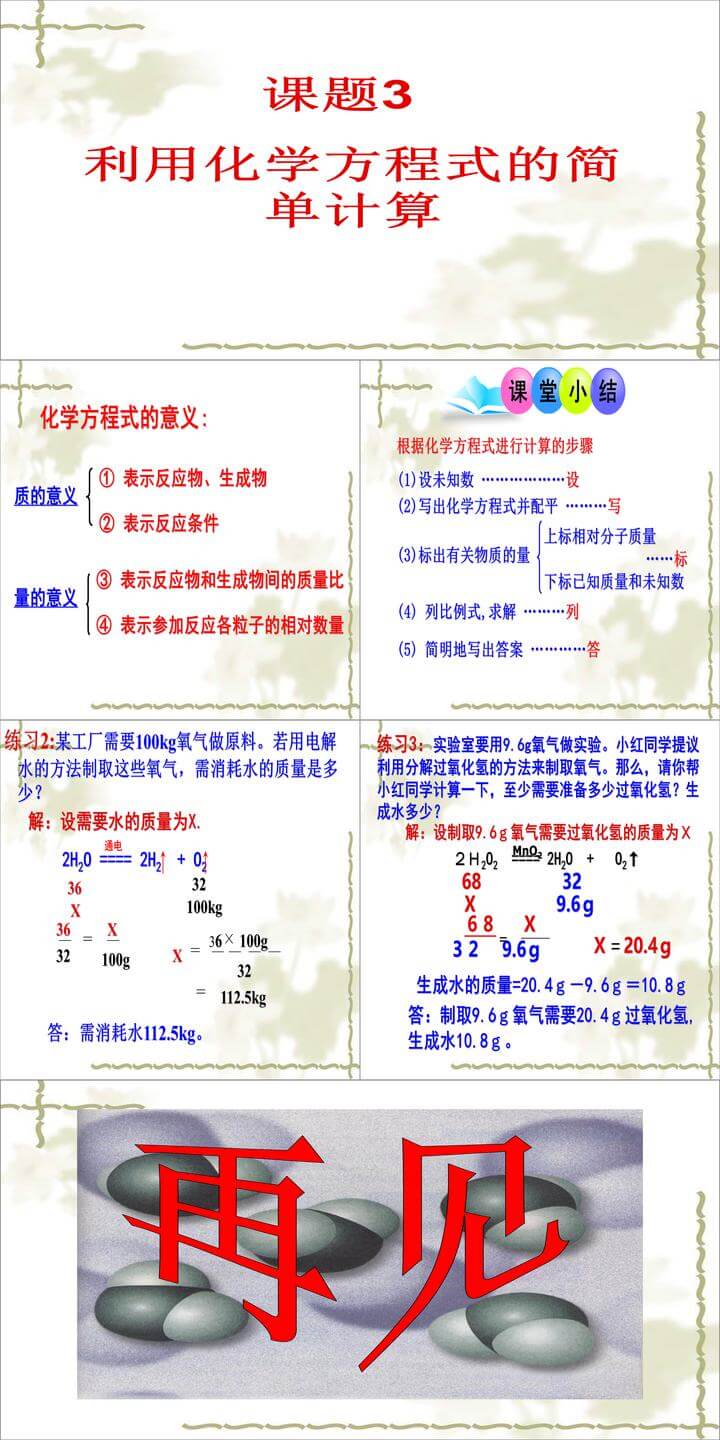
课题3:利用化学方程式的简单计算
(1)、表示反应物生成物及反应的条件。
(2)、表示各反应物、生成物之间的粒子个数之比。
(3)、表示反应物、生成物各物质之间的质量比。
复习提问:1、化学方程式的含义你清楚吗?
复习提问:以镁在空气中燃烧为例说明化学方程式的涵义。
镁在空气中燃烧反应中反应物与生成物之间的质量比可表示为:
2Mg + O2 → 2MgO
若:48克镁燃烧可生成80克氧化镁。
总结规律:在化学反应中,反应物与生成物之间的质量比成正比例关系。
因此,利用此正比例关系,根据化学方程式由一种反应物(或生成物)的质量,可求另一种生成物(或反应物)的质量。
【例 1】、加热分解6g高锰酸钾,可以得到多少克氧气?
解:设加热分解6g高锰酸钾,可以得到氧气的质量为x。
答:加热分解6g高锰酸钾,可以得到0.6g氧气。
一、已知反应物的质量求生成物的质量
(1)设未知量(未知数不带单位)
(2)写出化学方程式并配平
(3)计算相关物质的质量比
(4)标出已知量、未知量
(5)列出比例式
(7)简明地写出答案
【解题步骤】【书写格式】
练习1:15.5克红磷在氧气中充分燃烧,可生成五氧化二磷多少克?
练习2、加热分解12.25克氯酸钾,可得到多少克的氧气?同时生成氯化钾多少克?
二、已知生成物的质量求反应物的质量
例2:工业上高温煅烧石灰石(CaCO3)可制得生石灰(CaO)和二氧化碳,如果要制取10 t氧化钙,需要碳酸钙多少吨?
练习3:在“绿色氧化剂”双氧水(H2O2)的溶液中加入二氧化锰后,常温下即可产生大量氧气,若制取48g氧气需消耗纯净的双氧水多少克?
三、有关不纯反应物或生成物的计算。
1.化学反应方程式中不管是反应物还是生成物,代入的都是纯物质的质量.如果遇到不纯反应物或生成物,应将不纯物质换算成纯物质的质量.
2.不纯物质和纯物质质量间的换算.
纯物质的质量 = 不纯物质的质量 ×纯度(质量分数)
例5、足量的镁带在标准状况下与11.2升的氧气(密度为1.43g/L) 充分燃烧,可以生成多少克氧化镁?
四.关于质量和体积间的换算
注意:如果已知体积或要算体积时,要用密度公式换算成质量才代入。
练习4.实验室用13g锌粒与足量的稀硫酸反应制取氢气。(已知:Zn+H2SO4===ZnSO4+H2↑)
计算:(1)生成氢气的质量为多少克?(2)这些氢气在标准状况下的体积是多少升?(标准状况下,氢气密度为0.0899g/L)
归纳小结:化学方程式计算的注意事项
【三个要领】(1)步骤要完整(设、写、算、标、列、解、答);(2)格式要规范;(3)单位要统一,计算要准确(一般保留1位小数);
【三个关键】(1)准确书写化学方程式;(2)准确计算相对分子质量;(3)代入量均指纯净物的质量(单位要代入计算过程);
根据化学方程式计算的四种类型
1.已知反应物的质量求生成物的质量.
2.已知生成物的质量求反应物的质量
3.已知一种反应物的质量求另一种反应物的质量.
4.已知一种生成物的质量求另一种生成物的质量.
课堂练习
1.氢气在氯气中燃烧生成氯化氢气体,燃烧100g氢气需要氯气多少克?生成氯化氢气体多少克?(Cl—35.5 )
2.在实验室里用氢气还原氧化铜制取铜。若制取3.0g铜,需要氧化铜的质量是多少?
3.锌和盐酸(HCl)反应生成氢气和氯化锌。实验室里用3.7g锌与足量的盐酸反应,可制得氢气和氯化锌的质量各是多少?(Zn—65,Cl—35.5)
交流与表达:学完本课后,你有什么收获与启示?
1、化学方程式中,知道反应物(或生成物)的质量,可以利用物质间的质量比计算出生成物(或反应物)的质量。
2、利用化学方程式的计算格式要规范化。
3、利用化学方程式的计算可以加强生产的计划性,有利于合理的利用资源。
谢谢大家!
名称:课题3利用化学方程式的简单计算教研课PPT教学课件下载
学科:化学
类型:PPT课件
年级:初中三年级
版本:人教版
页数:21张
大小:448.67 KB
格式:pptx
预览图随机显示 6 页,实际是21页PPT。
下载链接中的资源是rar压缩包,解压缩后是ppt文档。
全站资源VIP会员免费下载。
购买之前建议先检测百度网盘链接是否失效。
部分精品课件来自优质公开课PPT,请勿公开传播。